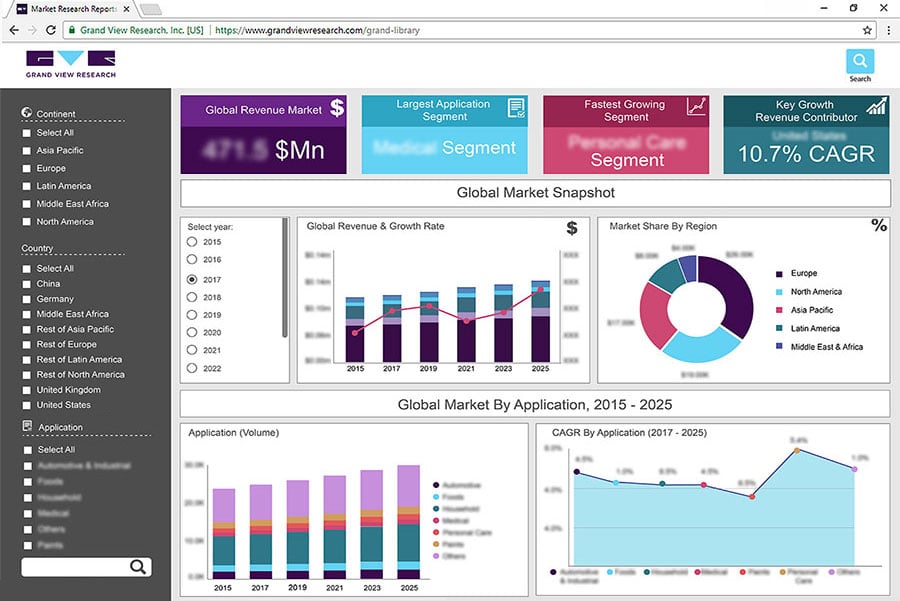
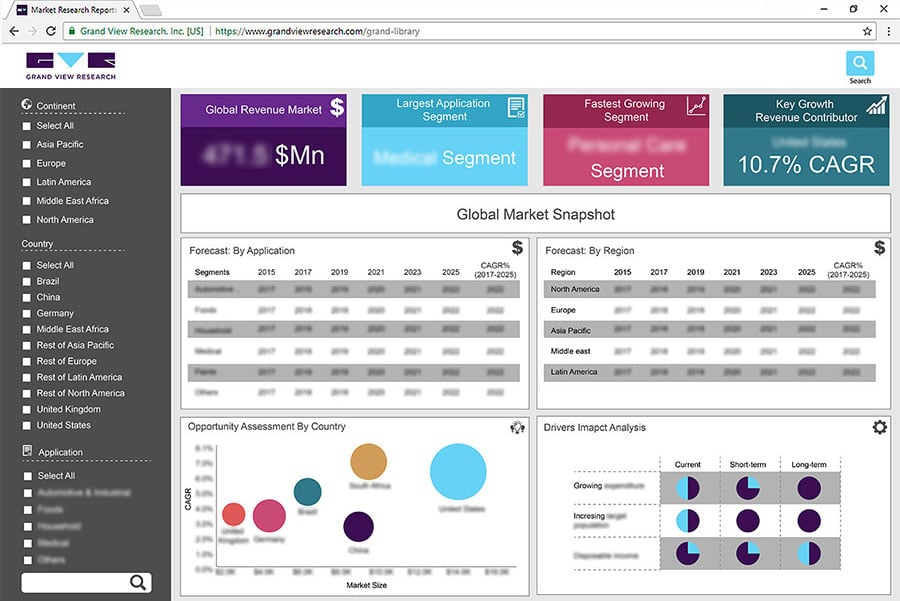
报告概述
2020年全球在研新药CDMO市场规模为42亿美元,预计2021年至2028年将以乐鱼体育手机网站入口6.9%的复合年增长率(CAGR)增长。市场的增长是由于制药公司外包服务的增加、研发投资的增加、临床研究的严格规定等因素造成的。FDA在新药开发中的作用开始于药物的发起人在筛选药物的药理活性和动物急性毒性后决定测试新分子在人类中的诊断或治疗潜力。根据联邦食品、药品和化妆品法案,这种分子改变了它的法律地位,成为一种受药品监管系统特定要求约束的新药。

根据大流行后的制药业前景,该行业将看到创新的增加,预计癌症和罕见疾病将受益最大。由于最近研究新药(IND)申请激增,预计合同服务将大幅增长,预计到2025年,FDA预计每年批准75个。从2020年4月到2020年6月,FDA收到了3806份IND申请,超过了之前8年的总和(2012-2019年为3576份)。
此外,2020年5月,FDA为COVID-19药物和生物制品的行业和研究人员发布了两份新的指导文件。FDA对抗击COVID-19的新治疗药物开发计划的期望在这两份指南中得到了强调,“COVID-19突发公共卫生事件:对COVID-19相关药物和生物制品ind前会议请求的一般考虑”和“COVID-19:开发用于治疗和预防的药物和生物制品”。
根据这份IND前指南,所有COVID-19药物开发相互作用都应通过IND会议请求启动,这是为了提供广泛的考虑,以协助申办者制定COVID-19相关药物的IND前会议请求。FDA建议通过Pre-IND项目提交药物开发申请,而不是通过pre-紧急使用授权,以提高IND提交的质量和内容,并简化潜在赞助商的投标。
IND申请和nda的审查和批准程序不断发展,从而影响批准趋势。2018年年中,FDA局长Scott Gottlieb宣布计划升级该机构的药物审查办公室,并发布了指导文件草案,说明FDA将如何在监管决策中纳入患者的意见。实际上,当涉及到监管批准时,FDA必须考虑标签外药物使用的真实证据。在评估药物批准时,FDA和其他监管机构会考虑患者报告的结果。
产品的见解乐鱼APP二维码
到2020年,小分子部分占据了89.0%的最大份额,并可能在预测期内保持主导地位。这在很大程度上是由于正在开发的小分子药物越来越多。目前市场上90%以上的药物都是小分子药物。2010年至2017年的7年间,美国FDA共批准了262个新型分子实体(nme),其中小分子占76%。此外,在2018年,小分子药物占fda批准药物的71%以上。
在整个预测期内,大分子部分预计将达到8.8%的最快复合年增长率。这在很大程度上是由于制药和生物技术公司在发现和开发大分子治疗蛋白方面投入了更多资金,因为它们具有特异性,可以针对以前难以解决的疾病状态,如肿瘤、神经病学和代谢疾病。预计到2020年,生物制剂在百强药品中的占比将从20%增加到50%。越来越多的制药和生物技术公司将有兴趣尽快将更多的创新生物治疗药物通过开发管道,外包为赞助商提供了在大分子领域竞争时立即获得扩大产能和专业知识的机会。
服务的见解乐鱼APP二维码
合同开发部门在2020年以85.5%的收入份额主导了市场。预计在预测期内,该细分市场也将以最快的复合年增长率增长。与内部药物开发相比,合同开发提供了一些好处,例如可以获得行业专家的帮助、更短的上市时间、成本效益,以及更专注于核心竞争力。大多数小型制药和生物制药公司由于缺乏内部能力而倾向于外包其药物开发活动。预计这将在预测期内推动市场。
预计在预测期内,合同制造部门将出现利润丰厚的增长。开发治疗药物的赞助公司正面临着控制成本和加快上市批准时间的巨大压力。虽然安全性和有效性最终决定了新药的成功,但其他因素,例如生产策略和执行,也会在很大程度上影响药物开发计划的成本和时间表。因此,赞助商选择对IND申请流程有全面了解的CMO是很重要的。
终端用户的见解乐鱼APP二维码
制药公司板块引领市场,2020年占69.4%。这可归因于制药部门投资的增加。大约有7000种不同的罕见疾病影响着全世界3.5亿人,人们正在进行比以往更多的研究。2017年,FDA批准了两种基于细胞的基因疗法,使基因和细胞疗法的正在研究的新药申请总数超过700个。

生物技术公司板块预计将在预测期内实现7.0%的丰厚增长率。基础研究既可以独立进行,也可以与来自生物医学研究生态系统各个部分(如疾病基金会和患者组织、风险资本和竞争前联盟)的研究人员和其他人合作进行。它面临着一个漫长的发展期,这是该领域所独有的。一个新药从申请IND到进入市场,在监管部门批准后,通常需要8年左右的时间。在这八年中,整个过程分为研究、测试和FDA评估三个阶段,所有这些阶段都有可能导致药物在任何时候失败。
区域的见解乐鱼APP二维码
到2020年,北美的份额最大,为41.1%。这可以归因于生命科学和制药企业的研发投资增加,预计这将增加该地区的合同制造需求。在美国,研究药物从实验室到药品柜平均需要12年的时间。每5000种经过临床前研究的药物中,只有5种能进入人体临床试验。FDA已经批准了五种药物中的一种,这些药物已经在人体中进行了测试。因此,一种新药进入市场的可能性只有五千分之一。
在整个预测期内,亚太地区预计将以7.7%的速度增长。欧洲和北美的生物技术公司正在扩大在该地区的业务。主要调查人员和杰出的意见领袖也大量涌入。各国政府一直在努力改善其监管体系,使其与欧洲和美国的标准更紧密地保持一致。因此,大中华区、韩国和新加坡等经济体获得了显著收益。
例如,在中国,自2016年以来,监管延误减少了16个月。中国国家药品监督管理局(NMPA)建议对临床优先适应症和突破性技术进行快速审查。最近,中国宣布了一系列改革措施,旨在改善药品审评流程,缩短修订(IND)和NDA申请所需的时间,并加速创新新药的开发。
关键公司和市场份额洞察乐鱼APP二维码
市场参与者正在实施一系列战略活动,例如新的伙伴关系协议、合作、合并和收购,目的是促进他们的服务和制造服务,以获得竞争优势。
例如,2021年6月,Charles River Laboratories International, Inc.收购了Vigene Biosciences, Inc.。此次收购扩大了其现有的细胞和基因治疗合同制造能力,并在美国提供了完整的基因修饰细胞治疗解决方案。全球研究性新药(IND) CDMO市场的主要参与者包括:
Covance Inc .)
查尔斯河实验室公司
Cambrex公司
IQVIA控股有限公司
Syneos健康
Lonza
康泰伦特
Recipharm AB
齐格弗里德控股公司
赛默飞世尔科技有限公司
研究性新药CDMO市场报告范围
报告的属性 |
细节 |
乐鱼体育手机网站入口2021年市场规模价值 |
43亿美元 |
2028年的收入预测 |
68亿美元 |
增长速度 |
2021年至2028年的复合年增长率为6.9% |
估计基准年 |
2020 |
历史数据 |
2016 - 2019 |
预测期 |
2021 - 2028 |
量化单位 |
收入(百万美元/十亿)和复合年增长率(2021 - 2028年) |
报告覆盖 |
收入预测,公司排名,竞争格局,增长因素和趋势 |
部分覆盖 |
产品、服务、最终用户、区域 |
区域范围 |
北美;欧洲;亚太地区;拉丁美洲;中东和非洲 |
国家范围 |
美国;加拿大;英国;德国;法国;意大利;西班牙;日本;中国;印度; Australia; South Korea; Brazil; Mexico; Argentina; South Africa; Saudi Arabia; UAE |
主要公司简介 |
Lonza;Catalent;Recipharm AB;齐格弗里德控股公司;赛默飞世尔科技公司;Covance Inc .);查尔斯河实验室;Cambrex公司;IQVIA Holdings Inc.;Syneous健康 |
自定义范围 |
购买时免费定制报告(相当于最多8个分析师工作日)。国家、地区、分部范围的增加或变更。 |
定价和购买选择 |
利用定制的购买选项,以满足您确切的研究需求。探索购买选择 |
报告所涵盖的部分
本报告预测了全球、地区和国家层面的收入增长,并提供了2016年至2028年每个子细分市场的最新行业趋势和机会的分析。为了进行这项研究,Grand View Research将全球下载乐鱼体育平台在研新药CDMO市场报告按产品、服务、最终用户和地区进行了细分:
产品展望(收入,百万美元,2016 - 2028)
小分子
大分子
服务展望(收入,百万美元,2016 - 2028)
合同发展
小分子
生物分析和DMPK研究
毒理学测试
病理学和安全药理学研究
原料药合成路线开发
原料药工艺开发
形式选择结晶过程发展
原料药的放大
之前的配方
临床前配方选择
首先是配方/工艺开发
分析方法开发/验证
原料药和制剂释放试验
制定净化步骤
伸缩和工艺改进
初步优化
原料药和制剂的形式稳定性
大分子
细胞系发育
过程开发
上游
微生物
哺乳动物
其他人
下游
马伯
重组蛋白
其他人
合同制造
小分子
口服固体
液体和半固体
注射剂
其他人
大分子
马伯
重组蛋白
其他人
终端用户展望(收入,百万美元,2016 - 2028)
制药公司
生物技术公司
其他(政府、研究机构、学术机构等)
区域展望(收入,百万美元,2016 - 2028)
北美
美国
加拿大
欧洲
英国
德国
法国
意大利
西班牙
亚太地区
日本
中国
印度
澳大利亚
韩国
拉丁美洲
巴西
墨西哥
阿根廷
中东和非洲
南非
沙特阿拉伯
阿联酋